- Qui sommes-nous ?
- Communiqués de ATMO GRAND EST
- Nos publications
- Assemblées Générales
- nos rencontres
- 13/06/2025 Initiation au golf
- 20/03/2025 visite ENDIVAL
- 09/02/2025 carnaval et bol d'air Jacquierl
- 05/01/2025 Galettes des rois à Bossendorf
- 26/01/2025 Théâtre à Entzheim
- 30/11/2024 Repas de Noël à Marlenheim
- 07/11/2024 Visite de Westhoffen
- 12/10/2024 Les arbres des 40 ans
- 22/08/2024 les buffonnes à Urhwiller
- 21/07/2024 barbecue à Saint Jean les Saverne
- 06/06/2024 écomusée Ungersheim
- 23/05/2024 carpes frites Château de Thanvillé
- 25/02/2024 carnaval à Bossendorf
- 01/01/2024 galettes à Bossendorf
- 02/12/2023 repas de Noël
- 16/11/2023 Est Fritures Wintershouse
- 12/10/2023 La Citadelle de Bitche
- 22/10/2023 Musée Agricole Allenwiller
- 22/08/2023 Visite distillerie HEPP
- 20/07/2023 Barbecue à l'étang de pêche
- 16/06/2023 Sortie sur le Rhin Romantique
- 22/05/2023 repas asperges
- 12/02/2023 rencontre asso.Osons
- 15/01/2023 Galette des rois à Molsheim
- 02/12/2022 Noël au Dôme Mutzig
- 201/11/2022 Loto a Kirchheim
- 20/10/2022 Chartreuse Molsheim
- 29/09/2022 Visite Musée Oberlin
- 29/07/2022 Pétanque à Dinsheim
- 19/05/2022 Musée de l'asperge
- 26/04/2022 Visite ferme Rothgerber
- 05/12/2021 Repas de Noël
- 12/11/2021 Manufacture des armes
- 22/08/2021 Barbecue à Traenheim
- 22/07/2021 Chemin des cimes
- 15/10/2020 confitures du Climont
- 14/08/2020 Plan incliné Artzwiller
- 24/07/2020 Visite des ruchers des Vosges du Nord
- 23/02/2020 Couscous Traenheim
- 19/01/2020 galette des rois Molsheim
- nos actions
- 15/05/2025 Azales Schirmeck
- 04/05/2025 Fête du souffle à Traenheim
- 25/04/2025 Alsace Cardio
- 16/05/2024 dépistage BPCO
- 26/04/2024 alsace cardio
- 05/03/2024 mesures souffle chez Heppner
- 20/06/2023 les infirmières asalees
- mai 2023 intiation au golf
- octobre 2022 balade Orangerie
- juillet 2020 marché de Schirmeck
- 09/03/2020 Journée du coeur à Strasbourg
- 11/2019 Mois sans tabac
- 14/11/2019 Partenariat ASLC
- 08/11/2019 journée BPCO 2019
- 01/09/2019 La couronne d'Or Marlenheim
- 07- 2019 2 premières réussies
- 14/06/2019 Le Bergopré Schirmeck
- 13/06/2019 Rencontre Club Albatros Lingolsheim
- 31/05/2019 Journée nationale sans tabac
- 28/04/2019 le défi de Jérémy
- 13/04/2019 Seniors et alors place Kléber Strasbourg
- 30/03/2019 Forum ADIRAL
- 22/02/2019 Journée du coeur
- 16/11/2018 Journée BPCO 2018
- 30/09/2018 Marche populaire à Bischwiller
- 21/09/2018 Alsace cardio à Colmar
- 23/09/2018 Rentrée des Associations 2018
- 03/06/2018 Slow Up à Scherwiller
- 18/05/2018 Seniors et alors !
- 27/04/2018 Forum NHC
- 07/04/2018 operation "Zéro mégots"
- 16/02/2018 journée du Coeur Strasbourg
- Séjours vacances
- Nouvelle page
- Chèques vacances ANCV
- Maladies respiratoires
- La BPCO par le Pr. E. WEITZENBLUM
- Emphysème
- Asthme : Allergies
- Syndrome d'Apnées Obstructives du Sommeil S.A.O.S
- Le SAOS chez l'enfant
- SOH Syndrome Obésité - Hypoventilation
- SED Syndrome d' Ehlers Danlos
- HyperTension Artérielle Pulmonaire H.T.A.P
- Cancer du poumon
- Pneumothorax
- Fibrose pulmonaire
- Bronchiolite
- Trachéotomie
- Mucoviscidose
- Acariens. Pr de Blay. Strasbourg
- Sarcoïdose
- Les traitements
- Vos droits et recours juridiques
- Activités physiques
- Ils témoignent
- La greffe devient urgente
- Un malade chanceux
- Apnée du sommeil chez l'enfant
- Au fil de l'eau Joaquim
- LE RAID AMAZONE
- Centre de santé Dieulefit
- Défier la BPCO par une activité physique quotidienne
- Pedaler pour vivre
- Vivre à pleins poumons
- Vivre avec une bronchite chronique, de l'emphysème et de l'asthme
- Vivre avec une fibrose pulmonaire
- Le benjamin de l’AMIRA
- Un grand réconfort
- BPCO: Bienfaits de la respiration abdominale
- Trucs et astuces
- Le quotidien d'un adolescent atteint de Myopathie de Duchenne
- Témoignage d'Albert 70ans
- "Charles Edouard" m'empoisonne la vie!
- "Renaissance"
- Nous rejoindre
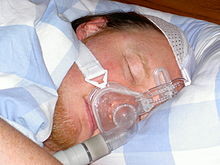
L’insuffisance respiratoire liée à l’obésité :
le syndrome obésité-hypoventilation
Emmanuel Weitzenblum, Service de Pneumologie, Nouvel Hôpital Civil, CHU de Strasbourg
La broncho-pneumopathie chronique obstructive (BPCO) représente de loin la première cause d’insuffisance respiratoire chronique (IRC). Cela est dû à sa grande fréquence (les statisticiens utilisent plutôt le terme de prévalence) puisqu’on estime que la BPCO est présente chez 5-10% des adultes de plus de 40 ans. Loin derrière la BPCO les causes importantes d’IRC sont les fibroses pulmonaires et le syndrome obésité hypoventilation (SOH) qui est l’insuffisance respiratoire des obèses. Il mérite d’être connu car il est loin d’être rare et, surtout, sa prévalence a augmenté de façon importante au cours des 30 dernières années, même si on ne dispose pas de données chiffrées précises. Le SOH est très souvent associé à un syndrome d’apnées obstructives du sommeil (SAOS) et il doit être recherché chez tout patient SAOS ayant une obésité prononcée.
1. Petit rappel historique et définition du SOH
Le SOH a été décrit il y a plus de 50 ans (1956) par des auteurs américains sous le terme de « syndrome Pickwickien ». En effet le tableau brossé par Charles Dickens du jeune garçon de ferme Joé, dans sa première nouvelle (1836) « The posthumous papers of the Pickwick Club » correspondait exactement à la présentation clinique de leur patient : Joé est sévèrement obèse, il a les jambes « enflées », il s’endort immédiatement après le repas et il est le plus souvent assoupi ou somnolent. Il présente donc les principaux signes du SOH qui se rencontrent également dans le SAOS.
Le syndrome de Pickwick a longtemps été considéré comme une affection rare, presque une curiosité. Le terme de syndrome obésité – hypoventilation (SOH) s’est progressivement substitué à celui du syndrome de Pickwick. Après 1956, les cas de SOH se sont multipliés, surtout depuis les années 1980 et on attribue logiquement cette progression à l’ « épidémie » d’obésité qui frappe le monde occidental depuis quelques décennies.
La recherche clinique a établi les relations qui lient l’obésité sévère au développement d’une insuffisance respiratoire hypercapnique associant baisse de la pression partielle d’oxygène du sang artériel (PaO2) et élévation de la pression partielle du gaz carbonique (PaCO2). Par ailleurs la documentation d’apnées au cours du sommeil chez les malades « Pickwickiens » a été obtenue dès 1965. Les malades « pickwickiens » (SOH) sont d’ailleurs les premiers chez lesquels les apnées ont été observées grâce à la polysomnographie débutante.
Dans les années 1990 et 2000 des études importantes ont été consacrées aux relations entre le SAOS et le SOH. Le renouveau indiscutable de l’intérêt pour le SOH au cours de la période récente tient d’abord à la fréquence aujourd’hui reconnue de cette affection qui représente, après la BPCO, l’une des premières causes d’IRC, et en second lieu à l’existence d’un traitement efficace, la ventilation non invasive.
On définit le SOH par l’existence d’une insuffisance respiratoire hypercapnique (hypoxémie + hypercapnie définie par une PaCO2 > 45mmHg) chez des patients obèses (index de masse corporelle > 30kg/m²) ne présentant pas d’affection respiratoire pouvant expliquer les anomalies des gaz du sang (BPCO par exemple). L’index de masse corporelle (IMC) est le rapport du poids en kilos sur le carré de la taille exprimée en mètres. Il est normalement de 20-25kg/m². A titre d’exemple, si le poids est de 70kg et la taille de 1,70m l’IMC est de 70/2,89 soit 24kg/m², il est donc normal. L’obésité est dite sévère lorsque l’IMC est supérieur à 40kg/m².
Le SOH n’est pas synonyme de syndrome d’apnées du sommeil même si les deux affections coexistent souvent : un SAOS est présent chez environ 80% des patients SOH.
2. Quelques données épidémiologiques
On ne dispose pas en fait d’études épidémiologiques fiables dans le SOH. On n’a donc pas une idée précise de sa prévalence (fréquence). On admet qu’il concerne moins de 10% des obèses sévères (IMC > 40kg/m²). Ce que l’on sait, c’est que la fréquence du SOH a augmenté de façon importante au cours des 20-30 dernières années, sans doute du fait de l’ « épidémie » d’obésité à laquelle sont confrontés actuellement tous les pays développés. A titre d’illustration nous avons colligé au niveau d’un service hospitalier de Pneumologie 62 nouveaux cas entre 1997 et 2002 et une centaine de cas supplémentaires entre 2002 et 2007. Le SOH n’est donc pas une affection rare. Des données épidémiologiques précises seront sans doute disponibles d’ici peu de temps.
Le SOH peut se rencontrer à tout âge et il a été décrit chez l’enfant, mais l’âge moyen de diagnostic est supérieur à 45 ans. Il est d’environ 60 ans dans notre série hospitalière signalée ci-dessus. Le SOH est un peu plus fréquent chez les hommes que chez les femmes.
La mortalité du SOH n’est pas bien connue. Elle est probablement élevée du fait de l’insuffisance respiratoire et des comorbidités associées à l’obésité.
3. Mécanismes de l’insuffisance respiratoire liée à l’obésité.
Dans ce domaine rien n’est établi de façon ferme en dépit des nombreuses études consacrées aux mécanismes de constitution d’un SOH. Schématiquement on peut envisager 3 causes principales qui peuvent d’ailleurs être associées :
Le coût excessif du travail des muscles respiratoires chez les grands obèses est sans doute le mécanisme principal de survenue de l’hypercapnie, mais il n’y a pas de relation linéaire entre l’importance de l’obésité exprimée par l’IMC et la fréquence du SOH dans une population donnée.
On a incriminé un dysfonctionnement des centres nerveux qui contrôlent la respiration. Ce dysfonctionnement, d’ailleurs difficile à mettre en évidence, n’est probablement pas le mécanisme principal.
Enfin, les apnées obstructives pendant le sommeil, qui sont présentes chez environ 80% des patients SOH pourraient contribuer à l’installation d’une hypoxémie- hypercapnie diurne. En effet, au cours des apnées nocturnes, surtout lorsqu’elles sont longues (> 30sec) il y a logiquement une chute de la PaO2 et une élévation de PaCO2. On peut envisager que cela peut conduire à la longue à une chute de la PaO2 et une élévation de la PaCO2 diurnes. En fait cette hypothèse n’a pu être démontrée de façon convaincante.
Les trois facteurs qui viennent d’être envisagés ne s’excluent certainement pas et, au contraire, leur conjonction peut favoriser la survenue d’un SOH.
4. Circonstances de découverte. Tableau clinique du SOH. Evolution.
Le diagnostic de SOH est d’ordinaire longtemps méconnu et souvent il n’est porté qu’à l’occasion d’une exacerbation de la maladie avec tableau d’insuffisance respiratoire sévère motivant l’hospitalisation en unité de soins intensifs, car les perturbations des gaz du sang artériel sont importantes (par exemple Pa02 < 55mmHg et PaCO2 > 60mmHg. Dans notre expérience presque la moitié des patients SOH ont été « découverts » dans ces circonstances.
Le diagnostic de SOH est en fait un diagnostic d’exclusion : mise en évidence d’une hypoxémie-hypercapnie alors qu’il n’y a pas de cause évidente des anomalies gazométriques en dehors de l’obésité.
Le signe fonctionnel le plus souvent rencontré est la dyspnée d’effort, souvent minimisée par les patients. L’obésité est présente par définition. L’IMC moyen de notre série de patients SOH est de 41 ± 7kg/m², ce qui indique qu’il y a beaucoup d’obésités sévères. Les malades SOH ont presque toujours des pathologies associées favorisées par l’obésité (on parle alors de comorbidités). Les plus fréquentes sont l’hypertension artérielle, les cardiopathies et le diabète de type 2 qui sont rencontrés dans 30 à 50% des cas. Ces comorbidités contribuent à la gravité du SOH.
L’association d’apnées obstructives du sommeil à un SOH est fréquente et il est nécessaire de rechercher les signes évocateurs d’un SAOS (ronflement, somnolence diurne etc…). Un examen polygraphique ventilatoire nocturne, voire une polysomnographie, est nécessaire dans tous les cas de SOH.
L’évolution du SOH dépend principalement de la sévérité de l’insuffisance respiratoire chronique souvent ponctuée par des épisodes d’insuffisance respiratoire aiguë. Le pronostic est lié tout autant aux comorbidités (par exemple une cardiopathie sévère) qu’à l’insuffisance respiratoire laquelle est largement accessible au traitement.
5. Principaux éléments du bilan
La mesure des gaz du sang artériel est indispensable au diagnostic puisque celui-ci repose sur la mise en évidence d’une hypoxémie-hypercapnie chez un obèse. L’oxymétrie de pouls est bien sûr insuffisante puisqu’elle ne permet pas de mesurer la PaCO2, se limitant à la mesure de la saturation en O2. Dans notre série personnelle, la PaO2 moyenne est de 59 ± 8mmHg et la PaCO2 de 50 ± 4mmHg ; ces données sont obtenues au cours d’une période stable de la maladie à distance d’une exacerbation.
Le diagnostic, on l’a vu plus haut, repose également sur l’exclusion d’une affection respiratoire chronique qui pourrait entraîner une IRC, une BPCO par exemple. Il est donc indispensable de pratiquer des explorations fonctionnelles respiratoires (EFR). Les EFR montrent l’absence de déficit ventilatoire obstructif qui pourrait orienter vers une BPCO. Dans le SOH on observe généralement un déficit restrictif avec une chute de la capacité vitale et de la capacité pulmonaire totale.
L’échocardiographie doit être pratiquée dans tous les cas pour estimer la fonction ventriculaire gauche car les patients SOH ont souvent une cardiomyopathie dite de l’obèse. Par ailleurs l’échocardiographie peut révéler une hypertension pulmonaire, conséquence fréquente d’une hypoxémie de longue durée.
La polysomnographie (enregistrement du sommeil et de la respiration ainsi que de la saturation transcutanée en oxygène) ou, à défaut, la polygraphie ventilatoire nocturne, doit être pratiquée dans tous les cas en raison de la fréquence d’un SAOS associé (voir plus haut) et parce que la mise en évidence d’un SAOS associé au SOH oriente l’attitude thérapeutique (voir plus bas).
6. Traitement
- La perte de poids est évidemment le traitement logique du SOH. Il est démontré qu’une perte de poids importante permet la correction de l’hypercapnie et qu’une perte de poids moins conséquente, mais d’au moins 10kg, entraîne une chute, mais non une normalisation de la PaCO2.
La chirurgie bariatrique (chirurgie de l’obésité) est couramment pratiquée aujourd’hui dans l’obésité sévère (> 40kg/m²) et peut être envisagée dans le SOH. Elle est le plus souvent refusée par ces patients d’un âge moyen déjà élevé (~ 60 ans) et de toute façon, certains patients, du fait des comorbidités et de l’âge, ne peuvent être candidats à la chirurgie bariatrique.
Il n’y a pas actuellement de traitement médicamenteux du SOH et les stimulants respiratoires se sont avérés décevants. Le traitement des comorbidités très fréquentes (HTA, cardiomyopathie, diabète) influence très largement l’espérance et la qualité de vie des patients SOH.
Il existe heureusement, aujourd’hui, une thérapeutique active du SOH qui est la ventilation nocturne, soit en pression positive continue (PPC), comme dans le SAOS (ce n’est pas alors une véritable ventilation nocturne) soit une ventilation à deux niveaux de pression, on parle alors de ventilation non invasive (VNI).
L’efficacité de ces traitements est démontrée : ils permettent de normaliser, ou en tout cas d’améliorer très nettement, la PaO2 et la PaCO2 de ces malades. Le traitement est nocturne, mais peut inclure les siestes.
Comment choisir entre PPC, traitement usuel du SAOS, et VNI, traitement de certaines insuffisances respiratoires sévères ? Si la polysomnographie documente la présence d’apnées obstructives, avec une fréquence significative, il est logique de débuter le traitement par la PPC qui est moins « lourde » pour le patient que la VNI. S’il n’y a pas d’apnées obstructives, éventualité observée chez 20% des patients SOH, il faut mettre en route une VNI, traitement un peu plus « invasif », mais globalement plus efficace. On entreprend également la VNI en cas d’hypercapnie importante (> 55mmHg) ou après échec de la PPC avec persistance de l’hypercapnie au bout de quelques semaines de traitement. Différents algorithmes de traitement ont été proposés et nous montrons (figure) celui que nous utilisons. La VNI est devenue le traitement de référence du SOH (en cas d’échec de la PPC) et les études récentes montrent que les résultats sont excellents avec amélioration de l’espérance de vie et de la qualité de vie.
7. CONCLUSION
Le SOH est une affection relativement fréquente. Il représente une des causes importantes d’insuffisance respiratoire chronique, loin derrière la BPCO il est vrai. Les apnées obstructives du sommeil SAOS sont présentes dans 80% des cas environ, mais SOH et SAOS représentent des affections distinctes, souvent associées, mais qui ne doivent pas être confondues. En l’absence de traitement médicamenteux le SOH bénéficie de la pression positive continue nocturne et, surtout, de la ventilation non-invasive dont les résultats sont excellents à moyen et long terme.
Figure
Algorithme que nous utilisons pour le traitement du SOH
Légende : PSG = polysomnographie, PPC = pression positive continue, VNI = ventilation non invasive, PaCO2 = pression partielle de gaz carbonique dans le sang artériel
PSG
↓
Apnées-Hypopnées obstructives
↙ ↘
OUI NON
↙ ↘
↓
PaCO2 < 50-55mmHg PaCO2 > 50-55mmHg
↓ ↘
PPC NOCTURNE VNI nocturne
↙ ↘
Si la PaCO2 est normalisée Si la PaCO2 ne varie pas
↓ ↓
Poursuite de la PPC Passage à la VNI
___________________________________________________________________________
